Hoe maak je een model van een molecuul van plasticine?

Scheikunde, gepresenteerd in saaie wetenschappelijke taal, zal een student waarschijnlijk niet interesseren. Maar als je visuele hulpmiddelen aansluit, wordt leren leuker. Het is nog interessanter om met uw eigen handen een lay-out te maken. In dit artikel vertellen we hoe je met plasticine een model van een molecuul kunt maken. Voor een informatieve les is de structuur van elk molecuul geschikt: ijzer, alcohol, koolstofdioxide. Laten we in meer detail stilstaan bij verschillende opties. Modellen van andere stoffen zullen volgens dezelfde regels worden uitgevoerd: we beeldhouwen atomen uit plasticine en voor structurele bindingen gebruiken we tandenstokers of lucifers.


Wat is er nodig?
Voordat u aan een modelleringsles en tegelijkertijd scheikunde begint, moet u de volgende materialen voorbereiden:
- plasticine van verschillende tinten;
- tandenstokers of lucifers;
- een bord of tafelzeil om met plasticine te werken;
- moleculaire formules van internet of een scheikundeboek.
Als alles klaar is, kun je beginnen met het maken van een moleculair model van elke stof.


Hoe verschillende modellen te vormen?
Het is beter om meteen een model van een molecuul van een bepaalde stof te boetseren volgens het schema dan te beginnen met uitleggen over micro-objecten van abstracte producten. Laten we eerst praten over de structurele bindingen van elementen aan de hand van het voorbeeld van verschillende stoffen: methaan, ethaan, ethyleen, methyleen.
Voor de duidelijkheid zullen we elk gefabriceerd molecuul wijzigen en er een diagram van het volgende cognitieve model van maken. Dit is niet moeilijk om te doen, omdat de binding van koolstof en waterstof bij alle schema's is betrokken.
methaan
Laten we eerst een eenvoudig molecuul van aardgasmethaan als basis nemen, het heeft de formule CH4. Om het bijbehorende model te maken, rol je vier kleine balletjes uit blauwe plasticine: ze stellen waterstof voor. Bereid vervolgens een rode bal voor, meerdere keren groter dan de blauwe, - koolstof. Maak structurele bindingen met lucifers en voeg waterstof toe aan koolstof 4. Het resultaat is het eenvoudigste model van een methaanmolecuul.


ethaan
De organische verbinding van ethaan C2H6 in de schematische versie ziet er ingewikkelder uit dan methaan, maar structureel is het model gemaakt van dezelfde plasticine onderdelen en lucifers, dus het zal niet moeilijk zijn om het te maken.
Verwijder een lucifer met het blauwe element uit de methaansculptuur. Hierdoor blijft koolstof over met twee waterstofbruggen. Voor de vorming van ethaan hebben we twee van dergelijke sets nodig. Door ze samen te binden met een extra lucifer, krijgen we een ethaanverbinding.


Ethyleen
Om ethyleen te modelleren, maken we een dubbele bindingsstructuur. Om dit te doen, verwijdert u van elke rode bal een lucifer met blauwe elementen uit het ethaanontwerp en voegt u een andere verbindingslucifer toe tussen de koolstofballen. Dit is wat we hebben.

methyleen
Nu, met behulp van het voorbeeld van methyleen (CH2), zullen we leren hoe we een keten van bindingen kunnen maken. Rol hiervoor 3 ballen van dezelfde grootte: een rode (koolstof) en 2 blauwe (waterstof).
We stellen een methyleenmolecuul samen met een dubbele binding en stellen een ketting samen volgens het volgende schema: waterstof-koolstof-waterstof, dat wil zeggen, we verbinden de blauwe bal met twee lucifers met een rode en opnieuw met twee lucifers met een blauwe bal. We zetten alle elementen op één lijn.

Voor cognitieve doeleinden stellen we voor om een aantal moleculen van verschillende chemicaliën te verzamelen.
Propaan
Dit gas behoort tot verbindingen met 3 koolstofatomen en 8 waterstofatomen (C3P8). Voor een ruimtelijk model moet je 3 grote rode ballen en 8 kleine blauwe erwten maken van plasticine. We hebben 10 lucifers nodig als verbindende banden. De assemblage van het propaanmolecuulmodel wordt op de volgende manier uitgevoerd.
- Met lucifers hechten we 3 blauwe erwten aan een van de rode bolletjes.
- We dupliceren de constructie, omdat we twee identieke opties nodig hebben.
- Voeg aan de resterende derde rode bal twee blauwe erwten toe die aan lucifers zijn bevestigd.
- Nu verbinden we alle drie de delen met elkaar. In het midden zou er een koolstofatoom moeten zijn met twee waterstofatomen, en langs de randen zou elke koolstof 3 waterstofatomen moeten hebben.
Het type bindingen dat verantwoordelijk is voor de structuur van het propaanmolecuul is hetzelfde als in de gassen van butaan, methaan.


Ammoniak
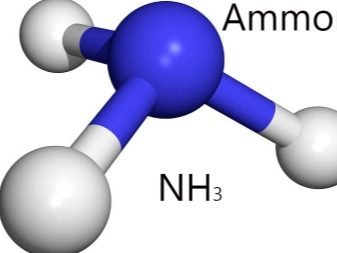
Het is een anorganische binaire verbinding van stikstof en waterstof (NH3). Ammoniak is een kleurloos gas dat gemakkelijk te herkennen is aan zijn karakteristieke geur. In eerdere modellen gebruikten we blauwe plasticine om het waterstofatoom te vormen en rood voor koolstof. Gebruik bij het modelleren van het ammoniakmolecuul ook blauw voor de drie waterstofatomen, dat wil zeggen, blind 3 blauwe ballen.
Kies voor stikstof een andere kleur zoals geel. Je hebt één bol van deze tint nodig. Bevestig nu met behulp van lucifers 3 waterstof (blauwe ballen) aan de stikstof (gele bal). Het ammoniakmodel is klaar.

Chloor
Dit halogeen is wijdverbreid in de omringende wereld. De moleculaire structuur van het gas is uiterst eenvoudig, het bevat slechts twee atomen (Cl2). Chloor is zwaarder dan lucht, heeft een groengele tint en een giftige, doordringende geur.
Het is niet moeilijk om de moleculen ervan weer te geven. Je moet twee groene ballen uit plasticine boetseren en ze verbinden met één lucifer. Een nog eenvoudigere manier is om twee ballen zijdelings aan elkaar te bevestigen zonder lucifers of tandenstokers te gebruiken.

Zout
Een complexe stof die in de natuur in verschillende varianten voorkomt, bijvoorbeeld natriumchloride (NaCl), calciumsulfaat (CaSo4). NaCl wordt ook wel tafelzout genoemd, ieder van ons is ermee bekend, omdat het geschikt is voor levensmiddelen.
Om een verbinding van tafelzout te maken, maken we twee ballen: klein groen (chloor) en groot bruin (natrium). Om er één molecuul van te maken, volstaat het om de balletjes tegen elkaar te drukken, maar je kunt ook een lucifer gebruiken, die de verbindende bindingen symboliseert.

Bruikbare tips
Moderne ouders weten hoe ze hun kinderen moeten ontwikkelen, zelfs zonder advies, maar we zullen toch enkele aanbevelingen doen.
Als je complexe informatie aan de student wilt overbrengen, zoek dan naar niet-standaard manieren om het te presenteren. In ons geval wordt scheikunde onderwezen door middel van 3D-modellering. De nuttige punten zijn als volgt.
- Kinderen leren nieuwe kennis.
- De methode om informatie te verkrijgen gaat gepaard met het creatieve proces van het beeldhouwen van volumetrische figuren. Het boeit en stelt de student in staat geïnteresseerd te raken in zo'n complex onderwerp als scheikunde.
- Werken met plasticine ontwikkelt handmotorische vaardigheden, dus het is nuttig voor mentale activiteit en creativiteit.
- Beeldhouwen helpt bij de ontwikkeling van nuttige eigenschappen zoals verbeeldingskracht, doorzettingsvermogen en concentratie.
Begin te leren met eenvoudige maar levensechte moleculaire modellen. Het kind moet zich onmiddellijk betrokken voelen bij echte wetenschap.
Nodig uw zoon of dochter uit om met behulp van een leerboek (internet) zelfstandig de formules te vinden van moleculen die u nog niet hebt gepasseerd. Laat het kind, met behulp van het gevonden schema en zijn fantasie, zonder hulp een model maken. Hij is misschien geïnteresseerd in de moleculen van lucht, zuurstof, water, goud, diamant of zoete suiker.


We maken verder een model van een watermolecuul van plasticine.








